こんにちは!ねこ太🐈です。
看護師国家試験にも毎年2~3問は計算問題が出ますよね。
計算問題は一応解けるけど、出た答えが本当に正しいか確信がもてない ( ̄∇ ̄|||)ってことは‥ないですか?

何となく公式に当てはめるけど、何でそういう式にするのか‥わからないまま解いてるかも‥。

確かに、結果的に解ければいいかもしれません。
でも、これから臨床で働くことを考えると、しっかり自信をもって答えが導き出せるようにしたいですね(*^_^*)
何でも、公式に当てはめるのではなく、中学レベルの基礎に立ち戻りながら‥『しっかり意味を理解して解く!』ということを一緒にやっていきましょう♪
今回は、濃度計算、その中でも‥「消毒液の希釈」「薬液投与」の計算について、バッチリ克服していきますよ~!
濃度計算(消毒液の希釈・薬液投与)に関する看護師国家試験問題を解いてみよう!
まず以下の2問を解いてみましょう。

もし分からなかったとしても、できれば‥「どうすれば解けるかな?」と少~し考えてみましょう!
なぜなら、悩むことが人の頭を一番賢くしてくれるからです。
看護師国家試験問題 (第104回 午後90問)
5%のクロルヘキシジングルコン酸塩を用いて0.2%希釈液2,000mLをつくるのに必要な薬液量を求めよ。
ただし、小数点以下の数値が得られた場合には、小数点以下第1位を四捨五入すること。
看護師国家試験問題 (第96回 午前27問)
250mg/5mLと表記された注射薬を200mg与薬するのに必要な薬液量はどれか。
1. 1mL
2. 2mL
3. 3mL
4. 4mL
今の時代は、投与する薬液がすでに生理食塩水などと混合されて投与しやすい形になった状態で販売されているので、臨床では‥確かに計算する機会は減りました。
でも、ゼロではありません。
そして、感染症が問題となっている昨今においては、消毒薬を毎日希釈して病床環境を消毒していたりします。
臨床で実施されていることが国家試験でもよく問われます!
なので、特に消毒薬の希釈などは‥しっかり解けるようにしておきたいですね♪
それでは‥ねこ太🐈と一緒に楽しく『広げ学習』をしながら、『知識』と『思考力』をサクッと身に付けていきましょうヽ(*^^*)ノ

『広げ学習』とは1問を解くことを通して、広~く深~く学習をして、3~4問解けるだけの知識を身につけていく学習のことです。(by ねこ太)
濃度計算(消毒液の希釈・薬液投与)に関する看護師国家試験問題の解説
いかがでしたでしょうか?
2問とも比較的解きやすい問題ではありますが、基礎を固めるためにはちょうどいい問題です。
最後にオリジナル問題も用意しましたので、ぜひ解いてみてください!
それも解ければ、「消毒液の希釈」「薬液投与」についてはバッチリでしょう♪
では、いきましょう!
看護師国家試験問題 (第104回 午後90問)
5%のクロルヘキシジングルコン酸塩を用いて0.2%希釈液2,000mLをつくるのに必要な薬液量を求めよ。
ただし、小数点以下の数値が得られた場合には、小数点以下第1位を四捨五入すること。
この問題を見たときに、どんなことをしているかイメージを持つことはできたでしょうか?
実は、計算問題ではイメージを持つことが、とても大切なポイントです。
私だったら‥こんなことをイメージします。


このイメージ図はすご~く大切なので、分かっていても描いておくと計算式を作ったりするときに、間違えることがなくなるので、オススメです!
ある量の「5%クロルヘキシジングルコン酸塩液」にある量の「水」を足して薄めた結果、「0.2%クロルヘキシジングルコン酸塩」が2000mlできたということです。

「ある量」という分からない部分は、とりあえず、それぞれ『X』と『Y』としてみましょう。
ここで方程式を立てます。

方程式って、『=(イコール)』で結んだ式のことでしたよね!

何がイコールで結べるのか‥クロルヘキシジングルコン酸塩液とか水の『量』かな?

そうですね!
確かに上の図では、希釈する前の溶液(5%クロルヘキシジングルコン酸塩液)と水の量の和と希釈してできた溶液(0.2%クロルヘキシジングルコン酸塩液)の量は等しくなっていますね。
なので、1つ式ができましたね。

【溶液の量が等しい】
(式1) X(ml)+Y(ml)=2000(ml)

単位ってとっても大切です。
もし問題文にできた溶液が2(L)となっていたら、単位をどちらかに合わせましょう。
基本は小数点以下の数字が出ない方が計算しやすいです。
なので、この場合は2000(ml)にした方がいいですね。
「溶液」とか「溶質」などの用語も出てきたので、サクッと復習しておきましょう♪
【溶液と溶質】
ある物質を溶かしてできた液体があったとき‥
溶けてできた液体⇒溶液
溶けている物質⇒溶質
(ちなみに‥溶かす前の元の液体⇒溶媒)
溶媒が水の場合の溶液を特に「水溶液」という。
(例)食塩水
食塩水が「溶液」で、溶けている食塩が「溶質」、水が「溶媒」となります。
そして、分からない数字が2つ(X、Y)とあるので、もう1つ式を立てると、連立方程式ができて療法とも出すことができそうです。
では‥何が等しいでしょう?

ひょっとして、ピンク色の部分の溶質!?

正解です!
ピンク色の部分はクロルヘキシジングルコン酸塩そのものです。
希釈する前の溶液に解けている溶質(クロルヘキシジングルコン酸塩)の量と、希釈した後の溶液に解けている溶質(クロルヘキシジングルコン酸塩)の量は等しいはずですね。
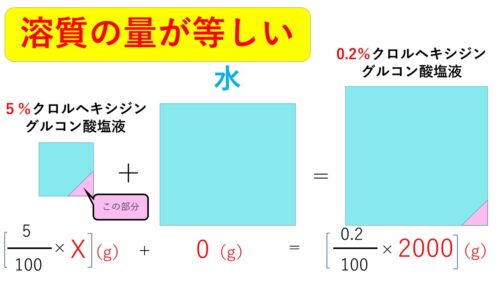

そっか‥加えた水の中には、溶質は溶けてないから、ゼロですね。
【溶質の量が等しい】
(式2) 0.05X(g)+0(g)=0.002×2000(g)

5%って‥0.05だっけ?
何で単位がg(グラム)に変わったんだろう?

パーセントは100分率で、100を全体としたときにいくつあるかってことだから、5%は「5/100」で「0.05」じゃないかな。それと0.2%の場合はは「0.2/100」。
100分率を掛けるときは、少数より分数で書いた方が間違えにくいかも♪

『%』って案外難しいですよね~。
看護師国家試験問題にも何の明記もない‥つまり常識として扱われている訳ですが‥
実は、『%』という単位は、ここでは明確に書かれていませんが、化学や物理の世界ではいろいろな意味があります。
【さまざまな%】
質量パーセント濃度⇒「溶液の質量」に対する「溶質の質量」の割合を100分率で表した濃度
(例)食塩水100gの中には食塩が10g溶けている⇒10%(厳密にはwt%)

wtは重さを意味する英単語「weight」に由来します。
体積パーセント濃度⇒全体の体積に対する「溶質の体積」の割合を100分率で表した濃度
(例)空気100L中には酸素が21L溶けている⇒21%(厳密にはvol%)

volは体積を意味する英単語「volume」に由来します。
質量対容量比濃度⇒溶液の体積に対する「溶質の質量」の割合を100分率で表した濃度
(例)食塩水100mlの中には食塩が10g溶けている⇒10%(厳密にはwt/vol%)

先程の重さを意味する「wt(weight)」と体積を意味する「vol(volume)」を組みわせたものです。
今紹介した3つの「%」の中で、上の問題で出てきた「%」はどの意味かというと‥質量対容量比濃度(wt/vol%)のことを指しています。

え~~そうだったんだ。一番難しそうだな‥って思ってたから違うのかと‥。

大丈夫ですよ!
そんなに難しく考えることはありませんからね。
看護師国家試験問題に出てくるのも、この質量対容量比濃度(wt/vol%)しか見たことがありません。
なので‥問題に「%」が出てきた場合は、基本的には‥質量対容量比濃度(wt/vol%)と考えてよいでしょう。
そして、もう1つ知っておかなければいけないことがあります。
それは以下のことです。
【質量対容量比濃度の「%」が意味すること】
体積の単位がml(ミリリットル)の場合、溶質の重さの単位はg(グラム)である。
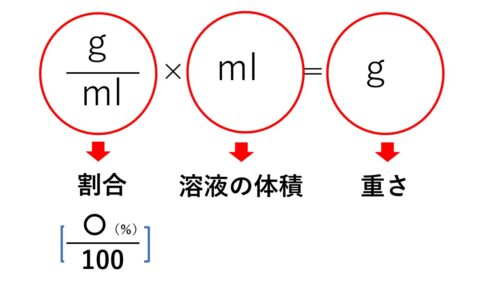
つまり、「%(パーセント)=g(グラム)/ml(ミリリットル)」ということになります。


そうなの‥なんか混乱してきたけど、そう覚えなければいけないのかぁ‥。

言葉で覚える必要はありません。
水1mlの重さは1gなので、mlとgは同じ様な単位として捉えておけばOKのです!
ちなみに‥もし体積の単位がℓ(㍑)であれば、重さの単位は㎏(キログラム)にすればいいだけです。※ℓ=1000ml、㎏=1000gだからです。

そっかぁ~牛乳パック1ℓはだいたい1㎏ですもんね。
そうやって考えれば「1ml」は「1g」って感覚も覚えやすいかも。
なので、「割合」に「溶液の量(体積)」を掛けたものは「重さ」になるという訳です。
では、先程の2つの計算式を解いてみましょう!
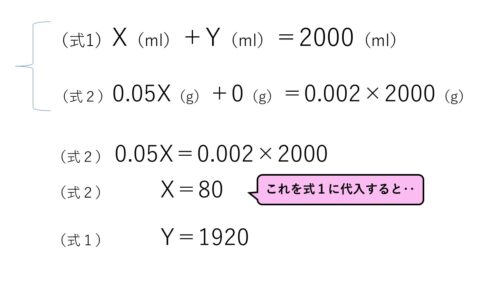

なるほど~こうやって出すのか~!

あれっ、(式1)がなくても(式2)だけで答えが‥80mlって出てる!?

その通りです。
実は、この問題では(式1)はなくてもよいのです。
ただ(式2)があれば‥、加える水の量を問われても、答えられます!
なので、一応‥式の立て方として【体積が等しい】として立てる式と、【溶質が等しい】として立てる式の両方を今回はやってみました。

どんな問題が来ても、バッチリですね!
ということで、答えは、「80ml」です。
では、次の2問目にいってみましょう!
看護師国家試験問題 (第96回 午前27問)
250mg/5mLと表記された注射薬を200mg与薬するのに必要な薬液量はどれか。
1. 1mL
2. 2mL
3. 3mL
4. 4mL
さぁ、この問題もイメージしてみましょう!

う~~ん、そうねぇ‥こんなイメージでいいのかな!?
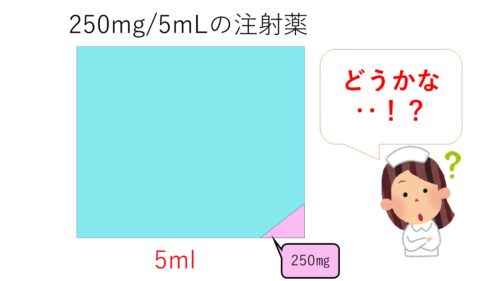

うん、きちんと何mlの薬液(溶液)の中に何㎎薬が溶けているか分かるように描けていますね!
いいですよ~!

ちょっと待ってください。
でも、これって全てを表しきれているのかな?
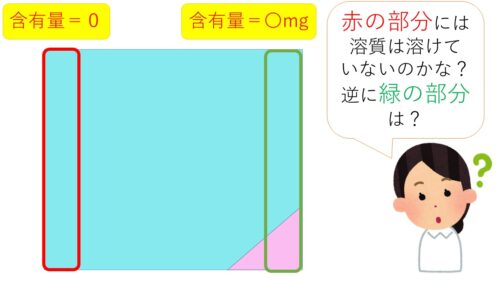

確かに‥そうだね。
これだと、場所によって濃度が違うね。
薬は均等に溶けているはずだから、変だよね~!

なるほど~。
では、均等に溶けているということを表現する図を一緒に考えてみましょう!

わたしは、こんな感じで考えてみました!
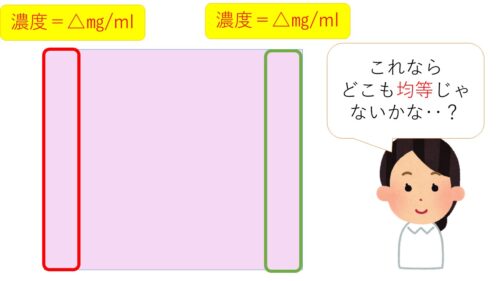

なるほど!
確かに均等ですね。
ただ、溶質が解けている量を視覚化しにくいかもしれません。

じゃあ‥こんなのはどうだろう!
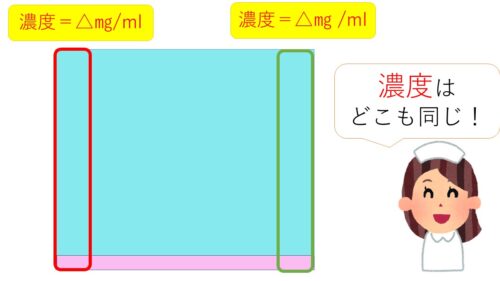

うん、これならいいかも!
ナス美は数学が得意なのね♪

ありがとう!
他の科目は‥全然ダメだけど、数学だけは得意なんだ~♪

得意なことがあるだけで、素晴らしいことですよ。
自分の得意な所‥強みを最大限活かしていくのは勉強をする上で大事ですね!
この図だと、濃度もそうですが‥溶液の量が変わったときに、溶けている溶質の量も変わることがイメージしやすいですね♪
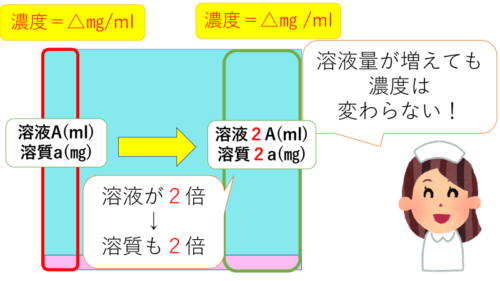
では、この図を元に考えてみましょう!
「250mg/5mLと表記されたを注射薬を200mg与薬する」とありますので、こんな感じになりそうです。
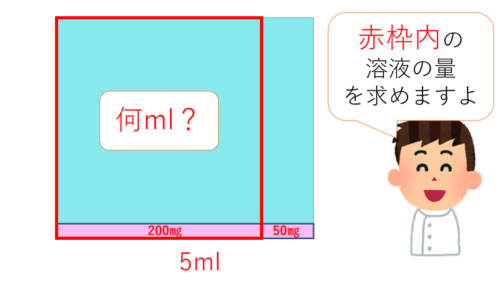
濃度はどこも一定ですので、「薬液(溶液)の量」と中にとけている「薬(溶質)の量」は比例します。
なので、「比」を用いて解いてみましょう!
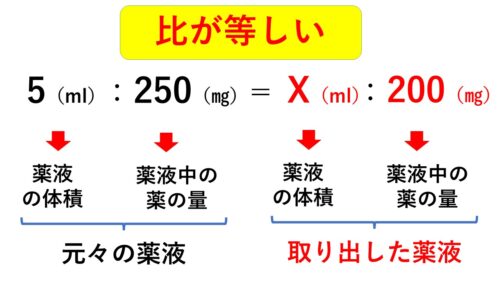
この比の式からXを計算すると‥


計算する際も、なるべく計算ミスを防ぐため、「5×200」のままにして、約分していくことがポイントです!
他にも方程式を使って解く方法もありますが、結果としては‥同じ式になるので、この解き方を基本として覚えておくと良いと思います。
ということで、答えは、「4ml」です。
ねこ太オリジナル確認問題
最後に、わたしが作成したオリジナル問題を1問解いてみましょう!
医師よりニカルジピン塩酸塩溶液(10㎎/10ml)4A(アンプル)を生理食塩液で希釈し、溶液400mlを作成し、輸液ポンプを用いて、ニカルジピン塩酸塩を1時間あたり2㎎の速度で投与する指示が出された。
問1.このときの注入速度(ml/時間)を求めなさい。

ちょっと複雑すぎる~。
こんなの臨床でやっているの?

大丈夫ですよ。
難しそうに見えても、やっていることは同じですから、まずは焦らないでいきましょう♪
ちなみに‥ニカルジピン塩酸塩溶液は、商品名でペルジピンという薬が超有名です。
これは血圧の薬‥さらにいうと降圧薬(Ca拮抗薬)です。
血圧が上がってしまった急性期の患者さんによく持続投与の指示が出されます。
計算はほぼ医師がしてくれているので、看護師はシリンジポンプに「〇ml/h」と入力するだけですが‥。
看護師も計算できるに越したことはありません。
患者さんに安全な医療を提供するため!
そして医師が間違えていたときに、実施した看護師の責任も問われかねないですからね‥自分の身も、医師の身も守っていきましょう♪
分からない人も‥できれば「5分」は考えてみましょう!
どこが分からないか明確にするだけでも、解説を読み終わった後に実力は「ぐぅ~ん」と伸びていますからね♪
では、解いていきましょう!

30分間考えて、こんなことをイメージしてみました!
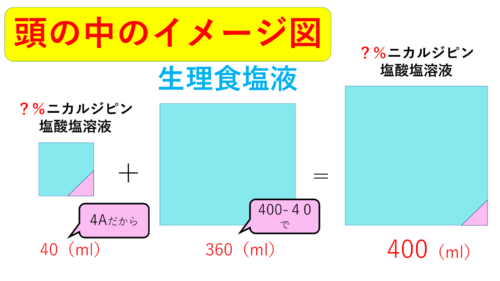

すごい!
確かに言われてみれば、そうだね。
図を描くだけで、生理食塩液の量まではスムーズに出ちゃうんだね。
でも、何%なのか‥出てないけど、いくつなんだろう?
ここでは、『%』までは出さなくても、解けてしまいますが‥でも、いい疑問なので考えてみましょう!
濃度については、以下のことがありましたね。
【質量対容量比濃度の「%」が意味すること】
体積の単位がml(ミリリットル)の場合、溶質の重さの単位はg(グラム)である。
つまり、%(パーセント)はg(グラム)/ml(ミリリットル)に変換して考えます。
ここでは、ニカルジピン塩酸塩溶液(2㎎/2ml)でしたので、「㎎」を「g」に直してみましょう。

m(ミリ)というのは、1㎜(ミリメートル)のミリと同じで、1000分の1という意味があります。
なので、「2㎎」は「2/1000g」ということになります。
とすると、アンプルに入っている原液の濃度は‥
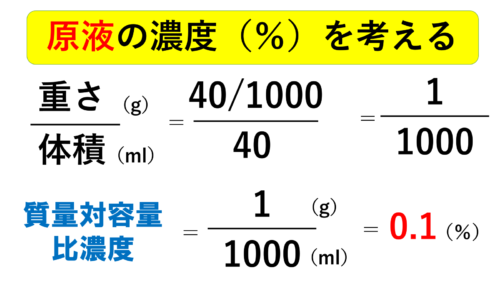
次に生理食塩液を入れて希釈した希釈液の濃度は‥


なるほど~。
確かに、ニカルジピンの添付文書にも「ニカルジピン塩酸塩として0.01〜0.02%(1mL当たり0.1〜0.2mg)溶液を点滴静注する。」と書かれている。
では、この先にいきましょう!
問題文に「ニカルジピン塩酸塩を1時間あたり2㎎の速度で投与する」とあります。

う~ん、わたしもここのイメージができなかったのよね。
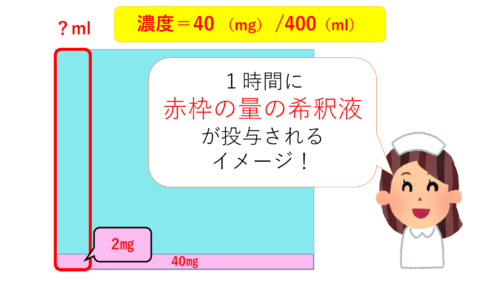
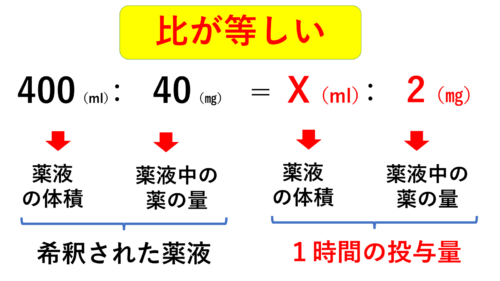
これを計算すると‥

答えは20ml/hですね!

自分たちの力だけで解けましたね!
素晴らしい~♪
さいごに♪
計算問題は何問か解くと、自分の感覚としても残ります。
問題集など解いてみたいという方は、トライしてみましょう!
でも無理に問題集をしなくても、ここで学んだ3問をしっかり解ければ、濃度計算(消毒液の希釈・薬液投与)はもうバッチリですので、自信をもって模試や国試に臨みましょう!
長くなってしまいましたが、最後までお読みいただき、ありがとうございました!
まずは、看護師国家試験合格‥そしてその先にある臨床で楽しく看護するための『力』をつけていくこと目標に、一緒にがんばっていきましょう!
〈その他のオススメ記事〉

↑ ↑ ねこ太の看護師国家試験勉強シリーズはこちら ↑ ↑







コメント
楽しく勉強させて頂いてます。
オリジナル問題の確認問題のところで1つ質問です。
最後の図の希釈された薬液の薬液中の薬の量は4mgだと思ったのですが、
40mgになる理由教えて頂きたいです。
ああああああ様
こんにちは。
ご質問頂きまして、ありがとうございます。
ご指摘頂いた通り、この問題であれば作成した薬液の中にニカルジピンが40mgではなく4㎎含まれているのが正しい事になります。
サイトに載せている図の量が間違っておりましたので、訂正したいと思います。
これからも勉強がんばってくださいね。
byねこ太